Objectif principal :
Comparer l’incidence des exacerbations cliniques sévères dans la prise en charge des ABPA, entre une stratégie avec un traitement d’entretien par Amphotéricine B liposomale nébulisé (LAmB) et une stratégie conventionnelle sans traitement antifongique d’entretien.
Objectifs secondaires :
-
Evaluer la tolérance des aérosols de LAmB,
-
Comparer entre les deux stratégies le nombre d’exacerbations cliniques sévères par patient,
- Comparer entre les deux stratégies l’incidence d’une aggravation de la symptomatologie clinique,
- Comparer entre les deux stratégies le nombre de consultations et d’hospitalisations pour des symptômes respiratoires entre M4 et M28,
- Comparer entre les deux stratégies la dose cumulée de corticoïdes systémiques et inhalés entre M4 et M28,
- Evaluer la concordance entre l’évolution de la symptomatologie clinique et les variations du taux des IgE totales ainsi que l’évolution des paramètres radiologiques
Critère de jugement principal :
Le critère de jugement principal est la survenue d’une exacerbation clinique sévère dans les 24 mois suivant le traitement d’attaque, définie par l’apparition ou l’aggravation d’une dyspnée par rapport à l’état de base ayant justifié :
1. une augmentation des traitements inhalés (bronchodilatateurs et/ou corticoïdes inhalés)
-et/ou la mise en route d’un traitement par corticoïdes systémiques
-et/ou une hospitalisation
2. ET persistante au-delà de 7 jours.
Seule la première exacerbation clinique survenant chez un patient sera considérée pour ce critère principal.
Critères de jugement secondaires :
Les critères de jugement secondaires sont :
1-Tolérance des aérosols évaluée notamment par la recherche de la survenue d’une dyspnée, toux, nausées, vomissements ou céphalées. Cette évaluation sera réalisée par le patient ou par l’infirmière au domicile du patient.
2- Le nombre d’exacerbations cliniques sévères survenant par patient pendant les 24 mois suivant la randomisation
3- La survenue d’une aggravation de la symptomatologie clinique définie par (un seul critère suffit)
· Une aggravation des symptômes cliniques définie par une augmentation du score évalué à M4 de 50% ou plus (Score évaluant chacun des symptômes suivants : toux, expectoration, sifflement, douleur thoracique selon une cotation de 0 à 3)
· et/ou une aggravation de la dyspnée évaluée par le score MRC
· et/ou une détérioration du contrôle de l’asthme évalué par l’investigateur selon les niveaux de contrôle définis par les recommandations du GINA.
· et/ou une détérioration du contrôle de l’asthme évalué par le patient à partir du Questionnaire ACQ5
4-Nombre de consultations ou nombre d’hospitalisations pour des symptômes respiratoires extraits du questionnaire ACQ-5
5- Dose cumulée de corticoïdes systémiques et inhalés (en équivalent prednisolone) de M4 à M28
6-Taux de concordance entre aggravation symptomatologique et
Variation des IgE totales par rapport M4
Evolution des paramètres radiologiques par rapport à M4 = modification cliniquement signifiante en nombre et/ou en étendu des anomalies radiologiques (évaluées par TDM-HR) en rapport avec l’ABPA..










 Cendrine GODET
Cendrine GODET Dr Gaël Dournes
Dr Gaël Dournes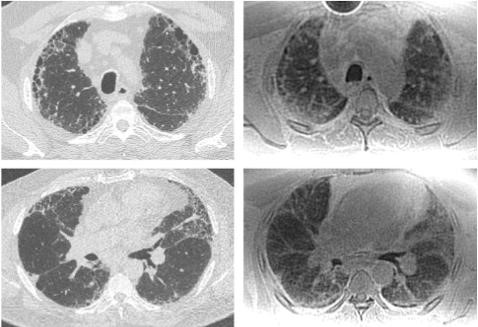
 Pr Anne BERGERON
Pr Anne BERGERON 

 Dr Drouot Xavier
Dr Drouot Xavier Pr Yves Jammes
Pr Yves Jammes  Dr Frédéric de BLAY
Dr Frédéric de BLAY Dr RIGAUD Pierre
Dr RIGAUD Pierre Dr Jean-Marc Naccache
Dr Jean-Marc Naccache Dr Rémi Coudroy
Dr Rémi Coudroy Pr. Bruno DEGANO
Pr. Bruno DEGANO Dr Louis MARQUESTE
Dr Louis MARQUESTE Dr SCHALLER Alexandre
Dr SCHALLER Alexandre